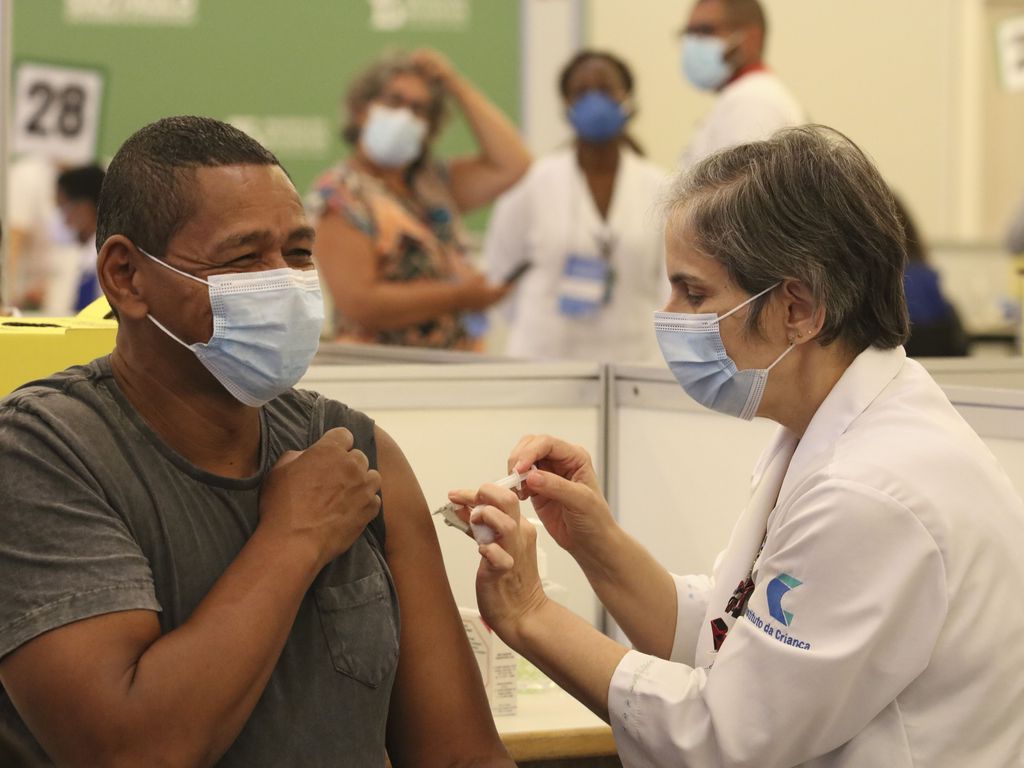
A parte polêmica do texto foi retirada pelo relator. Era a que permita que entidades privadas da área de saúde também pudessem comprar vacinas e administrá-las, enquanto os grupos prioritários estivessem sendo vacinados
A Câmara dos Deputados, finalmente aprovou, nesta terça-feira (23), o texto da MP (Medida Provisória) 1.026/21, que dá até sete dias úteis para Anvisa (Agência Nacional de Vigilância Sanitária) decidir sobre a aprovação temporária de vacinas contra a Covid-19 que tenham sido autorizadas por pelo menos uma entre 11 autoridades sanitárias estrangeiras.
O prazo, porém, pode ser estendido para até 30 dias caso faltem informações por parte da autoridade internacional. A matéria vai ao exame do Senado, que vai dar celeridade à discussão e votação do texto. Depois, vai à sanção presidencial.
A principal polêmica em torno do texto foi que no parecer preliminar do relator, deputado Pedro Westphalen (PP-RS), as entidades privadas da área de saúde também poderiam comprar vacinas e administrá-las, mas teriam de doar metade ao SUS (Sistema Único de Saúde) enquanto os grupos prioritários estivessem sendo vacinados. A oposição discordou e o relator retirou.
Entre outros pontos, a MP dispensa a licitação e prevê regras mais flexíveis para os contratos. O texto também retoma a autorização para que a Anvisa aplique rito sumário para vacinas e insumos aprovados por autoridades sanitárias dos Estados Unidos, da União Europeia, do Japão, da China ou do Reino Unido.
PARTICIPAÇÃO DO SETOR PRIVADO
Ao encaminhar o voto pela bancada do PCdoB, a deputada Alice Portugal criticou a “inépcia prolongada do governo federal no contrato das vacinas”. E na busca dessas “vacinas, vamos aprovar esta medida provisória”, disse. “Compreendemos, no entanto, que precisamos ressalvar destaques em relação à questão de o setor privado ter acesso prioritário, facilitado e isso gerar fura-fila gigantesca no Brasil. E isso para nós é muito sério e fortalecer o SUS é fundamental”, chamou a atenção.
“Por isso, vamos votar ‘sim’ pelo dinamismo, mas vamos ressalvar os destaques para a garantia do fortalecimento do SUS”, finalizou a parlamentar do PCdoB.
Para o deputado Jorge Solla (PT-BA), a medida encareceria a vacina e diminuiria a cobertura necessária do país. “Vender as vacinas vai arrefecer a pressão pela vacinação pública e vai aumentar os valores a serem pagos pelo setor público”, criticou.
Para o deputado Henrique Fontana (PT-RS), a solução para a vacinação do país “não é permitir um mercado privado de vacina”. Segundo ele, é fundamental a vacinação no setor público para garantir a imunização da população como um todo. Ele acusou o governo federal de atrapalhar o combate à pandemia.
SEM LICITAÇÃO
A MP permite que a aquisição das vacinas contra Covid-19 seja feita sem licitação, mesmo antes do registro ou autorização emergencial da Anvisa, devido à situação de emergência em saúde pública causada pelo novo coronavírus.
Outros insumos, como seringas e agulhas, e bens e serviços — de tecnologia, serviço, publicitário e treinamentos, por exemplo —, também estão incluídos, desde que relacionados à vacinação contra a Covid-19.
O texto também prevê a possibilidade de “cláusulas especiais” no contrato, como pagamento antecipado, inclusive com a possibilidade de perda do valor antecipado, e hipóteses de não penalização da empresa contratada.
O governo, porém, deve exigir medidas para reduzir o risco contratual, como a comprovação da execução de parte do produto para o pagamento antecipado e o acompanhamento do insumo durante o transporte.
A divulgação das contratações, com dados sobre a compra e a empresa, precisa ser feita na página oficial do órgão público na internet. Ainda segundo a proposta, os órgãos de controle devem priorizar a análise dos contratos firmados com base nessas regras excepcionais.
As regras valem para atos ou contratos firmados até 31 de julho deste ano, independentemente do prazo de execução ou de prorrogações.
AUTORIDADES ESTRANGEIRAS
O texto aprovado também aumentou o número de autoridades sanitárias estrangeiras que servem como base para a autorização temporária de vacinas ou outros medicamentos contra a Covid-19 feita pela Anvisa.
Pela proposta, a autorização será concedida “conforme estabelecido em ato regulamentar” da agência brasileira, que terá até sete dias úteis para a decisão final, desde que o imunizante tenha sido aprovado em pelo menos uma das agências internacionais abaixo:
1) Food and Drug Administration (FDA), dos Estados Unidos;
2) European Medicines Agency (EMA), da União Europeia;
3) Pharmaceuticals and Medical Devices Agency (PMDA), do Japão;
4) National Medical Products Administration (NMPA), da República Popular da China;
5) Medicines and Healthcare Products Regulatory Agency (MHRA), do Reino Unido e Irlanda do Norte;
6) Federal Service for Surveillance in Healthcare, da Rússia;
7) Central Drugs Standard Control Organization, da Índia;
8) Korea Disease Control and Preventiona Agency (KDCA), da Coreia do Sul;
9) Health Canada (HC), do Canadá;
10) Therapeutic Goods Administration, da Austrália; e
11) Anmat (Administración Nacional de Medicamentos, Alimentos y Tecnología Médica), da Argentina.
Outras autoridades sanitárias estrangeiras que tenham reconhecimento internacional também podem se encaixar nesta previsão.
Segundo o texto, um relatório técnico emitido pelas autoridades estrangeiras “deve ser capaz de comprovar que a vacina atende aos padrões de qualidade, eficácia e segurança” estabelecidos pela OMS (Organização Mundial de Saúde) e por outras convenções internacionais. Na ausência deste documento, o prazo de decisão da Anvisa passa a ser de até 30 dias.
O texto também retira a necessidade de que os testes de fase 3 sejam feitos no Brasil. A própria Anvisa já tinha anunciado essa desobrigação, no início de fevereiro.
DESTAQUES REJEITADOS
O destaque do PDT pretendia retirar do texto a permissão para contratos de compra de vacinas com pagamento antecipado, inclusive com a possibilidade de perda desse valor, e com cláusula de não penalização da contratada.
A emenda do deputado Enio Verri (PT-PR) pretendia incluir no grupo prioritário de vacinação as pessoas com deficiência, os profissionais de saúde, de educação, de assistência social e de segurança pública, assim como os profissionais que trabalhem ou sejam convocados a trabalhar nos serviços públicos considerados essenciais.
E a do deputado Danilo Cabral (PSB-PE) pretendia criar sistema de controle da fila de vacinação, com publicação das informações, assegurada a proteção de dados pessoais.
PROJETO DO PRESIDENTE DO SENADO
No Senado, o presidente da Casa, Rodrigo Pacheco (DEM-MG), apresentou, nesta terça-feira, projeto de lei (PL 534/21) que facilita a compra de vacinas contra o coronavírus por empresas privadas. O texto também permite que estados, Distrito Federal e municípios assumam a responsabilidade civil por eventuais efeitos adversos provocados pelos imunizantes. Essa medida abre caminho para a aquisição de vacinas por governadores e prefeitos.
Pelo projeto, os imunizantes comprados por pessoas jurídicas de direito privado devem ser integralmente doados ao SUS (Sistema Único de Saúde) e utilizados no âmbito do Programa Nacional de Imunizações. Só após a vacinação dos grupos considerados prioritários, as empresas seriam autorizadas a “adquirir diretamente vacinas para comercialização ou utilização”, determina a proposta.
“Identificamos a necessidade de permitir a participação complementar da sociedade civil neste processo tão desafiador. Com o intuito de ampliar a capacidade de compra e os canais de distribuição, autorizamos a aquisição direta de vacinas por entes privados para doação ao SUS ou para comercialização, desde que concluída a vacinação dos grupos prioritários”, afirma Rodrigo Pacheco na justificativa do projeto.
RESOLVER PROBLEMA QUE NÃO EXISTE
Ainda segundo o PL 534/21, Estados, Distrito Federal e municípios — e não apenas a União — ficariam “autorizados a assumir os riscos referentes à responsabilidade civil em relação a eventos adversos pós-vacinação”. Mas isso vale apenas para imunizantes registrados na Anvisa ou autorizados temporariamente para uso emergencial.
Pacheco propôs esta medida para resolver “problemas que não existem”, a fim de transpor as dificuldades criadas pelo governo federal, que combate as vacinas e a vacinação, num negacionismo criminoso.
“A escassez da oferta de vacinas, somada à necessidade de acelerar o processo de imunização não nos autoriza a dispensar nenhuma oportunidade de aquisição. Nesse sentido, propomos que a legislação autorize que possa o ente público assumir riscos e responsabilidades decorrentes de eventos adversos pós-vacinação, viabilizando, assim, o atendimento às condições atualmente impostas pelos fornecedores”, destaca Pacheco.
O texto permite que União, Estados, Distrito Federal e municípios constituam garantias ou contratem seguro privado nacional ou internacional “para a cobertura dos riscos”. A matéria aguarda distribuição para as comissões temáticas da Casa.
O relator da proposta vai ser o senador Randolfe Rodrigues (Rede-AP). “Acabo de assumir uma das principais responsabilidades na luta pela vacina no Brasil”, disse Randolfe em rede social, ao anunciar a relatoria do projeto de lei.
M. V.