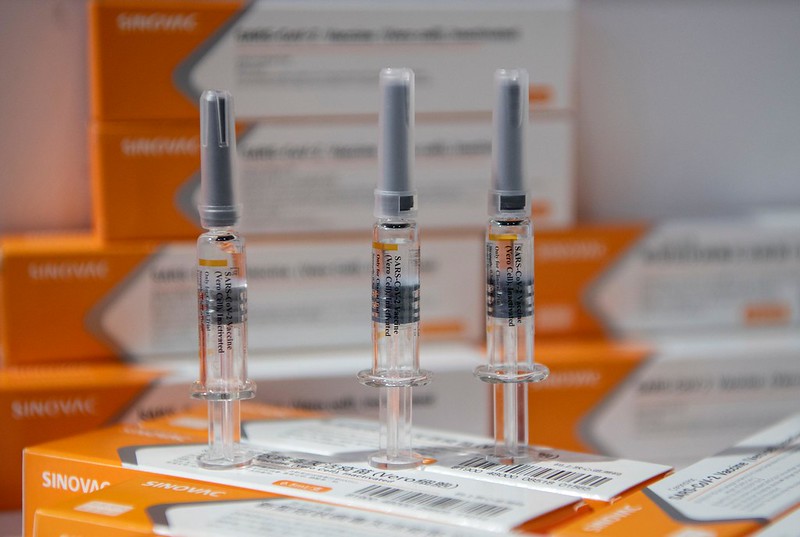
O governador de São Paulo, João Doria, confirmou que o Instituto Butantan iniciou o envio da documentação exigida pela Agência Nacional de Vigilância Sanitária (ANVISA) para o registro da vacina CoronaVac. O imunizante é desenvolvido pelo Butantan em parceria com laboratório chinês Sinovac.
“O objetivo é tornar o mais rápido possível, dentro das normas científicas e do protocolo da Anvisa, o processo de registro da CoronaVac, uma das vacinas mais promissoras na sua última etapa de testagem em todo o mundo”, disse o governador.
A documentação foi enviada por meio de uma plataforma digital da ANVISA para vacinas contra o coronavírus chamado de submissão contínua.
De acordo com o diretor do Instituto Butantan, Dimas Tadeu Covas, essa nova normativa da Anvisa facilita o fluxo de documentos para registro de vacinas para o coronavírus. “Foi estabelecido um fluxo contínuo e os documentos podem ser remetidos à medida que são gerados. Isso tem o objetivo de facilitar a análise dos técnicos, para que não tenha atraso nesse processo tão importante. Já submetemos os documentos disponíveis da nossa vacina à Anvisa. Isso mostra o comprometimento de que estudos de registro da vacina sejam feitos rapidamente”, afirmou.
Na última quarta-feira (30), o governo de São Paulo assinou um contrato com a Sinovac de fornecimento de 46 milhões de doses da CoronaVac até dezembro deste ano. Até o final do ano, a farmacêutica vai enviar 6 milhões de doses da vacina já prontas, enquanto outras 40 milhões serão formuladas e envasadas em São Paulo. Outras 14 milhões de doses devem ser fornecidas até fevereiro do ano que vem.
Na entrevista coletiva da assinatura do contrato, Doria afirmou que, se a CoronaVac passar na fase de testes em voluntários e for aprovada pela Anvisa, a vacinação poderá ocorrer já a partir de 15 dezembro e começará em profissionais de saúde de unidades públicas e privadas de saúde de São Paulo.
AMPLIAÇÃO DO ESTUDO
O estudo da vacina CoronaVac foi ampliado no país, passando de nove mil para 13 mil voluntários. Tanto na China quanto no Brasil, os testes clínicos passaram a envolver voluntários com mais de 60 anos. A Coronavac já vem sendo testada no Brasil desde julho e, atualmente, os estudos clínicos em voluntários acontecem em 12 centros de pesquisa em cinco estados e no Distrito Federal.
O governo de São Paulo já havia divulgado o resultado de um estudo feito em 50 mil pessoas na China que indicou segurança da Coronavac. De acordo com as informações, 94,7% dos voluntários não apresentaram qualquer efeito adverso – índice que se equipararia a outras vacinas já amplamente usadas no Brasil, como a da gripe. Mas os testes continuam e somente a partir de 15 de outubro que será possível começar a ter informações sobre a eficácia do imunizante.